
L’Agenzia Italiana del Farmaco ha pubblicato l’ottavo Rapporto di Farmacovigilanza sui Vaccini COVID-19. I dati raccolti e analizzati riguardano le segnalazioni di sospetta reazione avversa registrate nella Rete Nazionale di Farmacovigilanza tra il 27 dicembre 2020 e il 26 agosto 2021 per i quattro vaccini in uso nella campagna vaccinale in corso (qui tutte le analisi di Luca Fusarosu ViPiu.it, in home page di ViPiu.it tutti i dati in tempo reale di province e regioni italiane oltre che di singoli paesi del mondo. ndr).
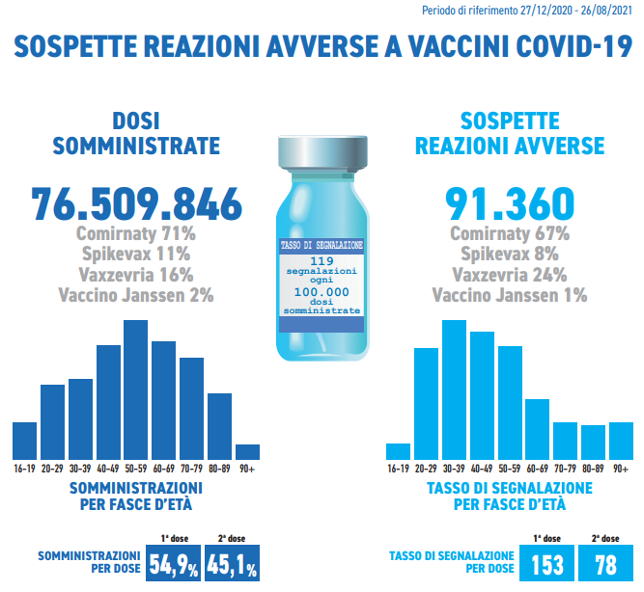
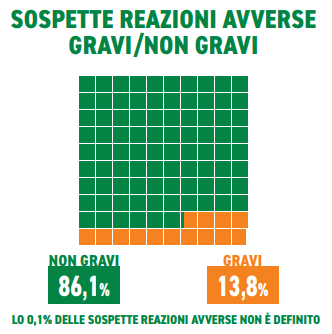
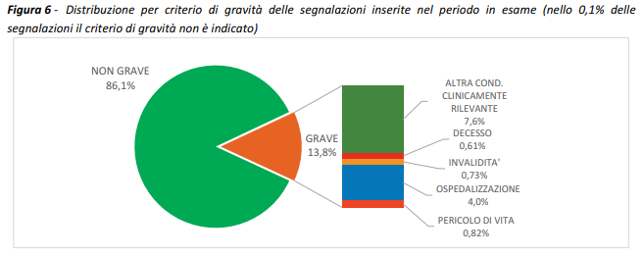
Nel periodo considerato sono pervenute 91.360 segnalazioni su un totale di 76.509.846 dosi somministrate (tasso di segnalazione di 119 ogni 100.000 dosi), di cui l’86,1% riferite a eventi non gravi, come dolore in sede di iniezione, febbre, astenia/stanchezza, dolori muscolari. Le segnalazioni gravi corrispondono al 13,8% del totale, con un tasso di 13 eventi gravi ogni 100.000 dosi somministrate.
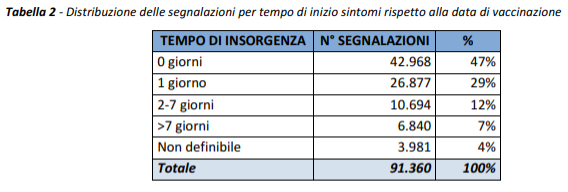
Come riportato nei precedenti Rapporti, indipendentemente dal vaccino, dalla dose e dalla tipologia di evento, la reazione si è verificata nella maggior parte dei casi (80% circa) nella stessa giornata della vaccinazione o il giorno successivo e solo più raramente oltre le 48 ore successive.
Comirnaty – BiOnTech Pfizer è il vaccino attualmente più utilizzato nella campagna vaccinale italiana (71%), seguito da Vaxzevria – AstraZeneca (16%), Spikevax – Moderna (11%) e Vaccino COVID-19 – Janssen (2%). In linea con i precedenti Rapporti, la distribuzione delle segnalazioni per tipologia di vaccino ricalca quella delle somministrazioni (Comirnaty 67%, Vaxzevria 24%, Spikevax 8%, COVID-19 vaccino Janssen 1%).
Per tutti i vaccini, gli eventi avversi più segnalati sono febbre, stanchezza, cefalea, dolori muscolari/articolari, reazione locale o dolore in sede di iniezione, brividi e nausea. In relazione alle vaccinazioni cosiddette eterologhe a persone al di sotto di 60 anni che avevano ricevuto Vaxzevria come prima dose sono pervenute 248 segnalazioni, su un totale di 604.865 somministrazioni (la seconda dose ha riguardato nel 76% dei casi Comirnaty e nel 24% Spikevax), con un tasso di segnalazione di 41 ogni 100.000 dosi somministrate. Nella fascia di età compresa fra 12 e 19 anni, alla data del 26/08/2021 sono pervenute 838 segnalazioni di sospetto evento avverso su un totale di 3.798.938 dosi somministrate, con un tasso di segnalazione di 22 eventi avversi ogni 100.000 dosi somministrate. La distribuzione per tipologia degli eventi avversi non è sostanzialmente diversa da quella osservata per tutte le altre classi di età.

L’86,1% delle reazioni sono considerate non gravi, il 13,8% gravi, lo 0,1% non definito
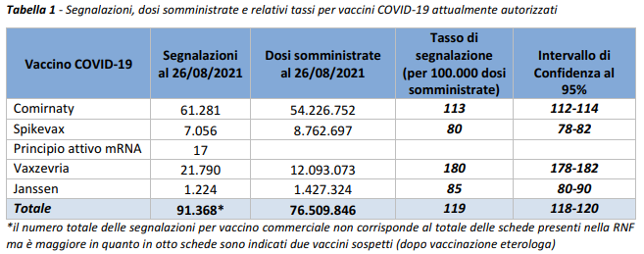
Il tasso di segnalazione è il rapporto fra il numero di segnalazioni inserite nel sistema di Farmacovigilanza rispetto al numero di dosi somministrate, al momento dell’estrazione dei dati. Questo valore viene riportato come numero di segnalazioni che si osservano ogni 100.000 dosi somministrate, in maniera tale da ottenere una misura standardizzata e confrontabile del funzionamento del sistema.
Comirnaty è il vaccino attualmente più utilizzato nella campagna vaccinale italiana (71%), seguito da Vaxzevria (16%), Spikevax (11%) e COVID-19 Vaccino Janssen (2%). In linea con i precedenti Rapporti, la distribuzione delle segnalazioni per tipologia di vaccino ricalca quella delle somministrazioni (Comirnaty 67%, Vaxzevria 24%, Spikevax 8%, COVID-19 vaccino Janssen 1%).
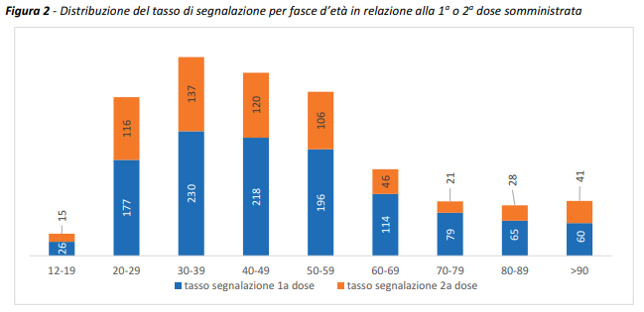
L’età media delle persone che hanno avuto un sospetto evento avverso è 48,3 anni (età mediana di 48 anni). Il tasso di segnalazione in base all’età e al numero di dose è riportato nella seguente figura:
La distribuzione delle segnalazioni in base al tempo di insorgenza rispetto alla vaccinazione è riportata in tabella 2.
La gravità delle segnalazioni viene definita in base di criteri standardizzati che non sempre coincidono con la reale gravità clinica dell’evento. Un evento è sempre grave se causa ospedalizzazione, pronto soccorso, pericolo immediato di vita, invalidità, anomalie congenite, decesso, altra condizione clinicamente rilevante. Alcuni eventi avversi, inoltre, vengono considerati sempre gravi se presenti in una lista pubblicata e periodicamente aggiornata dall’Agenzia Europea dei Medicinali, sotto il nome di IME list (Important Medical Events, per es. febbre alta).
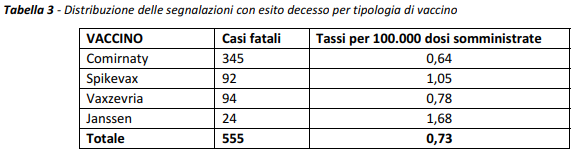
Complessivamente, 555 di queste segnalazioni gravi riportano l’esito “decesso”: il 48,5% dei casi riguarda donne, il 50,8% uomini mentre lo 0,7% non riporta questo dato.